二价钴离子水溶液颜色
电路板消费过程中,焊垫局部需求采用化学镀镍的办法先堆积上一层镍,再用化学镀金的办法堆积一层金,以进步耐磨性、降低接触电阻,从而利于电子元器件的焊接。漂洗水是化学镀镍产生的主要废水,其污染物以氨氮和镍为主,具有氨氮含量高、镍离子处于络合状态的特性。镍属于第一类污染物,氨氮是水体富营养化的主要缘由,假如处置不当,化学镀镍漂洗废水将形成严重的环境污染问题。依据《电镀污染物排放规范》(GB21900―2008)表2的请求,氨氮和镍的排放浓度分别为15mg/L和0.5mg/L,广东省珠三角地域以至请求到达表3的请求,氨氮和镍的排放浓度分别需求提标至8mg/L和0.1mg/L,氨氮和镍已成为电路板企业最难达标的污染物指标。
目前,化学镀镍污染管理主要集中于浓废液处置,而对漂洗废水的研讨较少,处置办法也主要集中于传统的化学沉淀法和化学氧化法。电催化氧化是一种高级氧化技术,能够在常温常压下以电子为主要反响对象对废水停止处置,是一种公认的绿色工艺,而采用电催化氧化处置氨氮废水更是环保范畴的研讨热点,但电催化氧化应用于化学镀镍高氨氮废水的处置却鲜见报道。
针对深圳市某电路板企业产生的化学镀镍高氨氮废水,笔者采用电催化氧化法对其停止处置,研讨了pH值、氯化钠投加量和电流密度对处置效果的影响,并对反响过程中pH值的变化和能耗停止了细致剖析,旨在为此类废水的处置提供参考。
1、资料与办法
1.1 实验资料
电催化氧化处置化学镀镍高浓度氨氮废水在自制循环式无隔阂反响槽中停止,实验安装由直流电源、反响槽、电极板、循环槽、循环泵和pH控制系统等6局部组成,实验安装见图1。反响槽和循环槽由聚丙烯资料制成,反响槽的内部尺寸为150mm×100mm×100mm,有效容积为1500mL;循环槽的内部尺寸为100mm×50mm×100mm,有效容积为500mL;阳极为Ti/RuO2-IrO2钛基电极,阴极为钛板电极,电极尺寸为100mm×95mm×1.0mm。
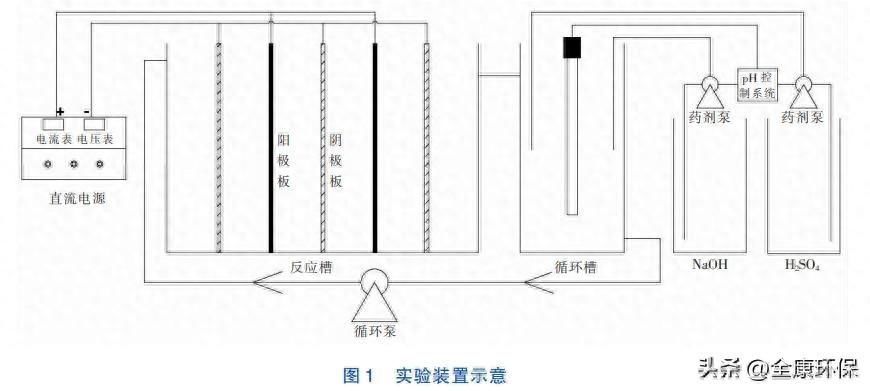
实验用水为深圳市某电路板企业化学镀镍漂洗废水,废水中氨氮浓度为4201.04mg/L,镍浓度为145.35mg/L,pH值为9.70,颜色为淡蓝色。
1.2 实验办法
每次用水量为2000mL,首先按设定投加量参加氯化钠,然后采用稀硫酸和氢氧化钠溶液调理废水pH值至设定值,将调理好的水样参加反响器中,采用循环处置方式停止实验,每隔一定时间从循环槽取样,测定样品中氨氮和镍的浓度。氨氮采用水杨酸分光光度法(HJ536―2009)测定,镍采用丁二酮肟分光光度法(GB/T11910―1989)测定。
本实验以氨氮的氧化降解状况核算反响过程的电流效率和能耗。电流效率η按式(1)计算,能耗W按式(2)计算。

式中:η为电流效率,%;C0为氨氮初始浓度,g/L;Ct为电催化氧化t时辰的氨氮浓度,g/L;F为法拉第常数,96485C/mol;I为电流强度,A;U为操作电压,V;t为反响时间,s;W为降解氨氮的能耗,kW•h/kg。
将式(1)代入式(2),得到式(3)。
由式(3)可知,降低电催化氧化处置氨氮废水的能耗能够有以下两种办法:①降低操作电压,在实践操作中能够经过进步废水电导率或降低极板间距完成;②进步电流效率,能够经过采用高催化活性电极或增加氯化钠投加量来完成。
2、结果与讨论
2.1 pH值的影响
2.1.1 pH值对氨氮降解和镍去除效果的影响
当氯化钠投加量为10g/L、电流密度为30mA/cm2时,调查pH值对处置效果的影响,结果见图2。从图2(a)可知,当pH值为8时对氨氮的降解效果最好,反响6h后出水氨氮浓度为1.34mg/L,远低于《电镀污染物排放规范》(GB21900―2008)表3中的限值。当pH值为6和10时氨氮的降解效果也较好,均能将氨氮浓度降至限值以下,但是效率低、耗时长,所以最适合的pH值为8。
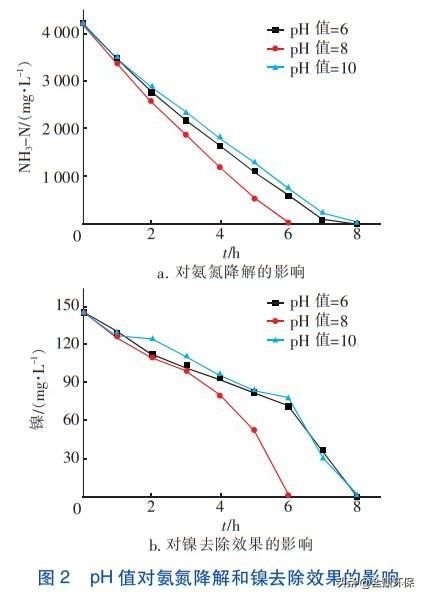
从图2(b)能够看出,对镍的去除能够分为两个阶段,前期去除速度迟缓,后期有一个明显的加速过程。分离氨氮含量的变化可知,镍去除速度的加快与氨氮含量降落存在关联,见式(4)~(6)。实验用水属于高氨氮含镍废水,废水中的镍根本上以镍氨络合状态存在,见式(4),随着氨氮的降解,式(4)均衡过程向左挪动,镍离子会逐步游离出来。此外,氨氮降解后,次氯酸根会逐步充裕,多余的次氯酸根能将二价镍离子氧化为三价,见式(6),而三价镍离子的沉淀pH值更低、沉淀更彻底。所以,镍的去除会延迟于氨氮的降解,且呈现明显的加速过程。当pH值为8时,出水镍浓度为0.08mg/L,低于《电镀污染物排放规范》(GB21900―2008)表3中的限值。
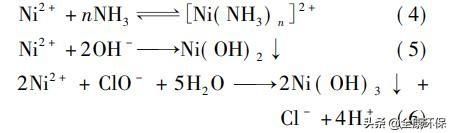
2.1.2 反响过程中pH值的变化
实验中发现,随着废水中氨氮的降解,pH值不时降落,为了恒定反响过程的pH值,需求不时向废水中投加氢氧化钠溶液。电催化氧化体系下的主要电极反响见式(7)和(8)。无隔阂电解槽内,阳极产生的氯气会很快与氢氧根发作反响,生成次氯酸根,见式(9)。次氯酸根氧化降解氨氮是电催化氧化条件下氨氮的主要降解途径,见式(10)。
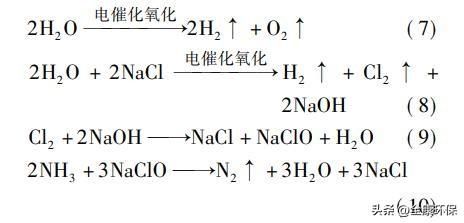
式(7)~(10)并未显现反响过程中pH值变化的缘由,剖析以为,应该与氨氮在废水中的存在状态有关,在本实验的pH值条件下,大局部氨氮以铵根离子(NH+4)方式存在,因而氨氮的降解反响见式(11),NH+4的H+在氨氮降解后会游离出来,应该是电催化氧化过程中pH值降落的主要缘由。
此外,若废水中的金属离子在阴极发作电解复原,会降低阴极析氢反响,形成H+累积,且金属离子的氢氧化物沉淀也会耗费废水中的氢氧根,见式(5)和(6),所以废水中金属离子的去除也会形成pH值的降落。
2.2 氯化钠投加量的影响
当电流密度为30mA/cm2、恒定反响过程中pH值为8时,调查氯化钠投加量对处置效果的影响,结果如图3所示。从图3(a)能够看出两个明显的现象:一是不同氯化钠投加量下,氨氮含量与反响时间近似成反比关系;二是随着氯化钠投加量的增加,氨氮的降解速度加快。这两个现象阐明,固定条件下氨氮降解的电流效率变化不大,且氯化钠投加量的增加可以进步电流效率,这也证明了在电催化氧化体系下氨氮主要经过间接氧化的方式降解。
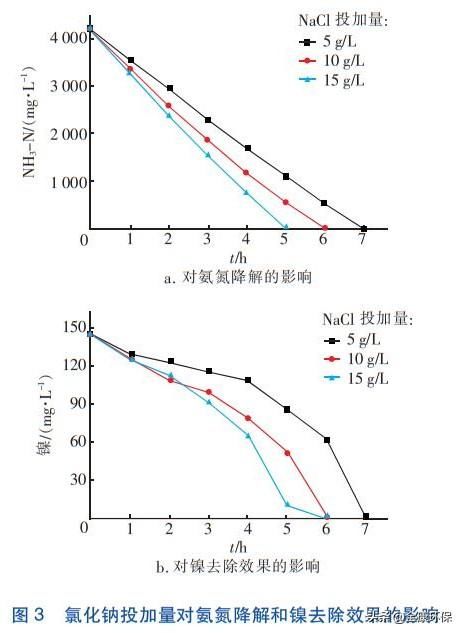
如2.1节所述,镍氨络合体系废除和镍离子氧化沉淀是去除镍离子的两个重要步骤,因而,镍离子的去除会滞后于氨氮的降解,且当绝大局部氨氮降解后,镍离子的去除会有一个加速过程,故氯化钠投加量越大,氨氮降解越快,从而镍离子的去除速度越快,见图3(b)。
2.3 电流密度的影响
当氯化钠投加量为10g/L、恒定反响过程中pH值为8时,调查电流密度对处置效果的影响,结果见图4。能够看出,电流密度越高,氨氮的降解速度越快。在电流密度为40mA/cm2的条件下,5h即可使出水氨氮浓度降为1.04mg/L;而当电流密度为20mA/cm2时,需反响8.5h才干使出水氨氮浓度降至1.02mg/L。
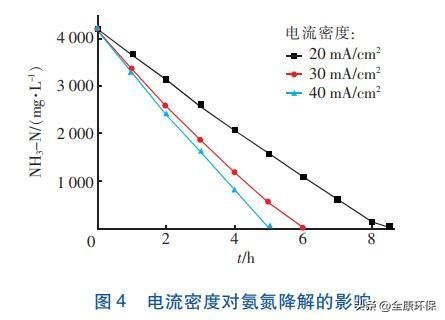
经计算,当电流密度为20、30、40mA/cm2时,相应的电流效率分别为70.60%、66.68%、50.00%。可见,电流密度越小,电流效率越高,这与相关文献报道分歧。当电流密度为40mA/cm2时,反响过程中能够明显察看到废水的温度急剧升高,阐明有一局部电能耗费在加热废水方面,但是电流密度太小会延长反响时间,关于极板面积一定的设备,电流密度低则会降低设备的处置才能。所以,实践操作中要综合剖析能耗和处置才能,以肯定适宜的电流密度,本实验肯定的最适电流密度为30mA/cm2。
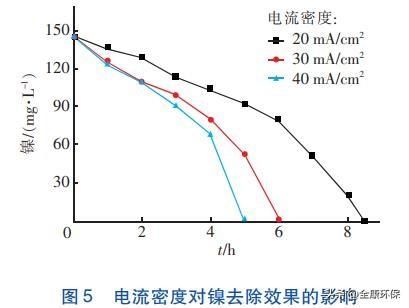
镍的去除过程与前面实验察看到的现象根本分歧,故在此不再赘述,详细浓度随时间的变化如图5所示。
2.4 能耗剖析
在初始氨氮浓度为4201.04mg/L、反响时间为6h、操作电压为4.5V、恒定pH值为8、氯化钠投加量为10g/L、电流密度为30mA/cm2条件下,出水氨氮浓度为1.34mg/L,电流效率为66.68%,降解1kg氨氮的能耗为38.74kW•h。
3、结论
采用电催化氧化法处置化学镀镍高氨氮废水,其最优pH值为8,反响过程中pH值降落的主要缘由是氨氮降解和镍离子去除;氯化钠投加量越大,氨氮降解速度越快;过高的电流密度会形成电流效率降落、能耗升高;镍的去除滞后于氨氮的降解。在最优实验条件下停止反响后,出水氨氮≤8mg/L、镍≤0.1mg/L,能够稳定到达《电镀污染物排放规范》(GB21900―2008)表3的请求,并提出了实践操作中降低能耗的可行办法,本实验中降解1kg氨氮的能耗为38.74kW•h。
","gnid":"9ef81c8402bbf3baa","img_data":[{"flag":2,"img":[{"desc":"","height":"391","title":"","url":"https://p0.ssl.img.360kuai.com/t012869b05e176ed5ba.jpg","width":"870"},{"desc":"","height":"126","title":"","url":"https://p0.ssl.img.360kuai.com/t010241180ed4b5dd3d.jpg","width":"433"},{"desc":"","height":"598","title":"","url":"https://p0.ssl.img.360kuai.com/t01e92c297a780910f0.jpg","width":"424"},{"desc":"","height":"133","title":"","url":"https://p0.ssl.img.360kuai.com/t010c7c6fcf5324b82c.jpg","width":"450"},{"desc":"","height":"223","title":"","url":"https://p0.ssl.img.360kuai.com/t018f1d56fa9c1a8314.jpg","width":"464"},{"desc":"","height":"633","title":"","url":"https://p0.ssl.img.360kuai.com/t0154aff44afba9294e.jpg","width":"462"},{"desc":"","height":"320","title":"","url":"https://p0.ssl.img.360kuai.com/t01529ccad4a5f9f339.jpg","width":"445"},{"desc":"","height":"308","title":"","url":"https://p0.ssl.img.360kuai.com/t0126da36a08c57ecad.jpg","width":"409"}]}],"original":0,"pat":"art_src_3,fts0,sts0","powerby":"pika","pub_time":1709879520000,"pure":"","rawurl":"http://zm.news.so.com/0b5f1da9b04b3f5e45678fa3a12f12f7","redirect":0,"rptid":"8f90a8f6bb20f0eb","rss_ext":[],"s":"t","src":"全康环保","tag":[],"title":"化学镀镍高氨氮废水处理电催化氧化技术
长闵苇3474Co(H2o)6 2+离子是什么颜色 -
尹卢咽17656443900 ______ 中文名称六水合钴(Ⅱ) 溶液中是粉红色,如果溶液浓度较大时略显紫红色
长闵苇3474帮忙归纳下初中化学中离子的颜色 格式:Cu,显 - 2价时,显蓝色 -
尹卢咽17656443900 ______ Cu,显+2价时,显蓝色 Fe,显+3价时,呈黄色溶液 Fe,显+2价时,呈浅绿色溶液 高锰酸根,呈紫红色溶液 初中记住这几个就行了
长闵苇3474我想明白钴和钴盐的颜色 -
尹卢咽17656443900 ______ 一、颜色不同 1、钴:有光泽的钢灰色金属.纯度较高的金属钴是浅玫色的灰色金属. 2、钴盐:玫瑰红色单斜晶体. 二、外文名不同 1、钴:Cobalt. 2、钴盐:cobalt salt. 三、应用不同 1、钴:生产耐热合金、硬质合金、防腐合金、磁性合金和各种钴盐的重要原料.金属钴主要用于制取合金.钴基合金是钴和铬、钨、铁、镍组中的一种或几种制成的合金的总称.是各种高级颜料的重要原料. 2、钴盐:钴盐用于增进橡胶与金属的粘合,已得到普遍认可并广泛应用于子午线轮胎和钢丝胶管等产品中.钴盐可以单独直接加入橡胶中作为橡胶与金属粘合的增进剂. 参考资料来源:搜狗百科-钴 参考资料来源:搜狗百科-钴盐
长闵苇3474求中学阶段所有有颜色的溶液,标明溶剂,颜色,特征 -
尹卢咽17656443900 ______ 溶剂均为水 二价cu离子的盐溶液(例cucl2)-----蓝色 二价fe离子的盐溶液(例feso4)------黄色 三价fe离子的盐溶液(例fecl3)-----浅绿色 高锰酸钾溶液-----紫红色 硫氢化铵+fe^3+-----血红色 Br2水溶液-----橙红色 只能想起来这些了,余下的找参考书或自己做题积累吧!
长闵苇3474Cu的化合物的颜色和其水溶液的颜色? -
尹卢咽17656443900 ______ 二价铜离子一般水溶液的颜色是蓝色的 不过CuCl2 在浓度很高时显绿色 还有一个在含有二价铜离子的溶液中滴加氨水颜色会由蓝色变成绛蓝色
长闵苇3474请问 Mn2+溶液是甚么颜色? -
尹卢咽17656443900 ______ 无色,(高锰酸钾有颜色)
长闵苇3474高中化学中、有颜色的一些特殊元素、离子、化合物、和水溶液 -
尹卢咽17656443900 ______ 首先纠正一个普遍的误区:三价铁离子的水溶液颜色是黄色,但三价铁离子是紫色的,离子颜色和溶液颜色大多数相同,并不全相同.铜离子及其溶液是蓝色的(先不考虑氯化铜,它有些特殊,大学后才接触) 亚铁离子及溶液浅绿色 二价锰离子是粉红色,但溶液在高中说成是无色至浅粉色 高锰酸根(Mn7价)离子及溶液是紫黑或紫红 离子和溶液一般就这些.化合物就多了:(我就说说离子推断中) 氯化银白色 溴化银淡黄色 碘化银黄色 钡离子,钙离子,镁离子沉淀都白色 氢氧化铜蓝色,氢氧化铁红褐色,锰酸钾(锰6价)绿色 过氧化钠浅黄色. 气体:二氧化氮红棕色,氯气黄绿色,碘蒸气紫黑色 如有不足之处,使你未能明白,欢迎你到百度“霸道一班”贴吧发帖提问交流
长闵苇3474化学题求解(关于钴的配合物性质)二价钴的氢氧化物,羟基配合物各是什么颜色,是否溶于水? -
尹卢咽17656443900 ______[答案] 钴 cobalt 一种化学元素,化学符号Co,原子序数27,原子量58.9332,属周期系Ⅷ族.1735年瑞典G.布兰特从辉钴矿中还原... 在简单化合物中以+2价最稳定,简单的+3价钴离子是强氧化剂,容易被还原.钴有三种氧化物:CoO、Co2O3、Co3O4.氢氧...
长闵苇3474哪些金属离子的水溶液有颜色,铍、银、锂、锶有颜色吗我说的是在水溶液中稳定存在时的离子的颜色. -
尹卢咽17656443900 ______[答案] 不少金属离子是有颜色的,比如二价铜离子(蓝色),农药波尔多液中就有硫酸铜,还有二价铁离子(绿色)三价铁离子(黄色),铬离子(蓝色)等等,铍、银、锂、锶离子在大多数化合物中是没有颜色的, 我说的是在稳定溶液中的状态
长闵苇3474分析溶液中钴离子浓度时,遇到很多颜色变化无法解释,目前正在做一个分析镍钴混合液中钴含量分析的实验,实验做了很多,碰到的颜色可谓是色彩斑斓,... -
尹卢咽17656443900 ______[答案] 滴定Co3+不需要加氨水缓冲溶液.pH~5-6即可. 加氨水(pH=10)会形成不同颜色的顺,反异构体 [Co(NH3)4(H2O)2]3+,[Co(NH3)4(H2O)Cl]+,[Co(NH3)4Cl2]+,和氢氧化钴等.