金属与硝酸反应
你可能知道,金属元素有不同的活泼程度,有些金属很容易与其他物质发生反应,有些金属则很难被氧化或还原。那么,如果让两种不同活泼性的金属相遇,会发生什么呢?今天,我们就来看看铜和硝酸银之间的反应,它是一种典型的置换反应,也是一场金属之间的较量。

什么是置换反应?
置换反应是指一种单质与一种化合物作用,生成另一种单质与另一种化合物的反应。例如,铁钉放在蓝色的硫酸铜溶液中,会发生如下的反应:
Fe+CuSO4=FeSO4+Cu
这个反应中,铁钉与硫酸铜溶液中的铜离子发生了置换,生成了硫酸亚铁溶液和红色的铜粉。我们可以看到,溶液的颜色由蓝色变成了淡绿色,而铁钉表面覆盖了一层红色沉淀。

铜和硝酸银之间为什么会发生置换反应?
我们知道,硝酸银是一种无色晶体,它能够溶于水,形成无色透明的溶液。硝酸银溶液中含有大量的银离子(Ag+),它们具有较强的氧化性,并且对有机物有腐蚀作用。如果我们把一根铜丝放入硝酸银溶液中,会发生什么呢?
Cu+2AgNO3=Cu (NO3)2+2Ag
这个反应中,铜丝与硝酸银溶液中的银离子发生了置换,生成了硝酸铜溶液和银白色的金属银。我们可以看到,溶液的颜色由无色变成了蓝色,而铜丝表面附着了一层亮闪闪的固体。
那么,为什么会发生这样的反应呢?原因就在于金属元素的活泼性不同。活泼性是指金属元素在氧化还原反应中失去电子(被氧化)或得到电子(被还原)的能力。铜比银活泼,
所以铜能够抢走硝酸银中的银离子,让它们变成单质的银。这样,一个氧化还原反应就完成了。
那么,在实验现象上,我们又能看到什么呢?首先,我们要知道硝酸银是一种无色晶体,它能够溶于水,形成无色透明的溶液。硝酸银溶液中含有大量的银离子(Ag+),它们具有较强的氧化性,并且对有机物有腐蚀作用。如果我们把一根铜丝放入硝酸银溶液中,会发生什么呢?
我们会看到,在铜丝与硝酸银溶液接触的地方,很快就会出现一层亮闪闪的固体。这些固体就是单质的银,它们从溶液中沉淀出来,附着在铜丝上。随着时间的推移,这层固体会越来越厚,直到把整根铜丝都包裹起来。这时候,我们就可以用镊子把这根“变成”了银的铜丝取出来,看看它的外观和质量。
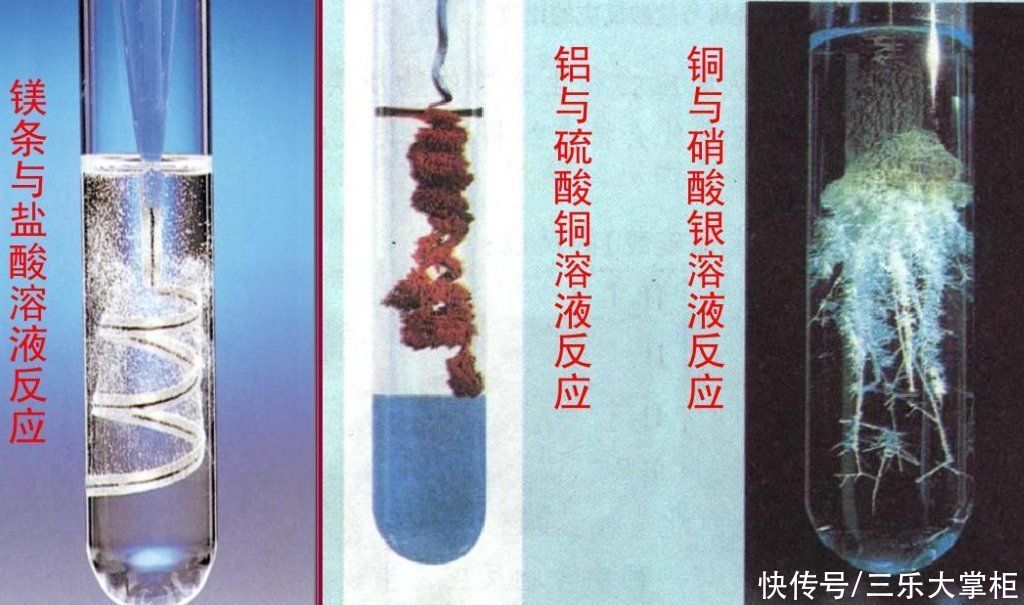
铜和硝酸银之间的反应应用和意义
铜和硝酸银之间的反应不仅是一种有趣的化学现象,也是一种有用的化学方法。我们可以利用这个反应来制备金属银,或者用来检验铜的纯度。我们还可以利用这个反应来制作一些美丽的工艺品,或者用来进行一些科学探究。
例如,我们可以用这个反应来制作一些银镜。银镜是一种镀有一层金属银的玻璃,它能够反射光线,形成清晰的影像。我们可以把一块玻璃放在一个装有硝酸银溶液和少量葡萄糖的容器中,然后把一根铜丝悬挂在溶液上方。这样,就会发生如下的反应:
Cu+2AgNO3=Cu (NO3)2+2Ag
C6H12O6+6O2=6CO2+6H2O
在这个反应中,铜丝与硝酸银溶液发生了置换反应,生成了金属银;而葡萄糖与溶液中的氧气发生了氧化反应,生成了二氧化碳和水。这样,就会在玻璃上形成一层均匀而细腻的金属银膜,也就是银镜了。

我们还可以用这个反应来制作一些有趣的图案或文字。我们可以在一张纸上用蜡笔画出我们想要的图案或文字,然后把纸浸泡在硝酸银溶液中,再把纸贴在一块铜板上。这样,就会发生如下的反应:
Cu+2AgNO3=Cu (NO3)2+2Ag
纸上没有蜡笔覆盖的地方会被硝酸银溶液渗透,然后与铜板发生置换反应,生成金属银;而纸上有蜡笔覆盖的地方则不会被硝酸银溶液渗透,也不会发生置换反应。这样,就会在纸上形成由金属银组成的图案或文字,而周围则是白色的纸张。
通过这些例子,我们可以看到,铜和硝酸银之间的反应不仅能够展示化学原理和现象,也能够激发我们的创造力和想象力。我们可以利用这个反应来进行更多的探索和实践,发现更多的化学乐趣。
","gnid":"95516b3c6010f446c","img_data":[{"flag":2,"img":[{"desc":"","height":"571","title":"","url":"https://p0.ssl.img.360kuai.com/t01e143a67e7033ee84.jpg","width":"946"},{"desc":"","height":"675","title":"","url":"https://p0.ssl.img.360kuai.com/t01b34335a1d8252502.jpg","width":"1188"},{"desc":"","height":"605","title":"","url":"https://p0.ssl.img.360kuai.com/t0103f64c28612552e4.jpg","width":"1024"},{"desc":"","height":"599","title":"","url":"https://p0.ssl.img.360kuai.com/t012dbc0746a67173cf.jpg","width":"1029"}]}],"original":0,"pat":"art_src_3,fts0,sts0","powerby":"cache","pub_time":1684250760000,"pure":"","rawurl":"http://zm.news.so.com/5fd87d41edc67e064cceb7ddbb130071","redirect":0,"rptid":"340dfddca20936da","rss_ext":[],"s":"t","src":"三乐大掌柜","tag":[],"title":"铜和硝酸银:一场金属之间的较量
任眨瑶3167金属与硝酸的反应 -
禹关味13359959257 ______ Fe+6HNO3(热、浓)=Fe(NO3)3+3NO2↑+3H2O 4Fe+10HNO3(冷、稀)=4Fe(NO3)3+NH4NO3+3H2O 4Fe+10HNO3(热、稀)=4Fe(NO3)3+N2O↑+5H2O 3Fe(过量)+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O 3Zn+8HNO...
任眨瑶3167高中化学 金属和浓 稀硝酸反应的条件和产物 谢谢! -
禹关味13359959257 ______[答案] 一般地说,浓硝酸(12~16mol/L)的与金属反应,不论金属活泼与否,它被还原的产物主要是二氧化氮;稀硝酸(6~8mol/L)与不活泼金属(Cu等)反应,主要生成一氧化氮,与活泼金属(Zn等)反应,则可能生成一氧化二氮或铵盐;与极稀的硝...
任眨瑶3167硝酸与金属反应的一系列计算 -
禹关味13359959257 ______[答案] 硝酸与金属反应发生的是氧化还原反应,必须满足得失电子数相等. 硝酸的总量= 起酸性作用的硝酸 +起氧化作用的硝酸+不参加反应(剩余)的硝酸 起酸性作用的硝酸生成盐 如硝酸铜 Cu2+:NO3-=1:2 起氧化作用的硝酸生成氮的氧化物 如NO3:NOx=1...
任眨瑶3167金属与硝酸反应
禹关味13359959257 ______ 16~12mol/l 时NO2 6~12 mol/l 时 NO 再稀还会生成N2 NH4+ 等
任眨瑶3167浓硝酸是否可与金属单质反应? -
禹关味13359959257 ______[答案] 浓硝酸可以与金属单质反应,但与一般酸不同的是,它与金属反应一般不生成氢气,而是生成二氧化氮.例如:Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
任眨瑶3167金属与硝酸反应的规律 -
禹关味13359959257 ______[答案] 生成硝酸盐+(浓酸二氧化氮)+(稀酸一氧化氮)+水
任眨瑶3167硝酸与金属氧化物反应的一般规律 -
禹关味13359959257 ______[答案] 若氧化物中金属元素以处于最高价,则直接发生简单的复分解反应,生成该金属的硝酸盐和水;若其金属不处于最高价,如氧化亚铜Cu2O,那么硝酸的氧化性非常强,会将该金属元素氧化至最高价,此时的产物除了该硝酸盐和水外,还有NO或NO2...
任眨瑶3167硝酸与金属反应 -
禹关味13359959257 ______ 硫酸不会和铜反应,但是硫酸里的氢离子会和硝酸根离子结合成硝酸就可以反应了. n(HNO3)=0.1mol/L*1L=0.1mol n(H2SO4)=0.4mol/L*1L=0.4mol 所以n(H+)=0.9mol n(NO3-)=0.1mol 铜足量 X 写出离子方程式 3Cu + 2NO3- + 8H+ = 3Cu2+ + 2NO + 4H2O Xmol 0.1mol 0.9mol 看方程是硝酸不足量按硝酸计算 X=0.1 m(CU)=0.1mol*64g/mol=9.6g
任眨瑶3167哪些金属单质与稀硝酸反应生成氢气,又有哪些金属与稀硝酸反应生成一氧化氮 -
禹关味13359959257 ______[答案] 所有的金属与稀硝酸反应都不生成氢气,因为金属有还原性,而稀硝酸是氧化性的酸,具有强氧化性,所以不生成H2,生成氮氧化物. 生成NO的金属有:除Pt,Au外金属.
任眨瑶3167金属铜和浓硝酸、稀硝酸反应的方程式如下:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O (NO、NO2气体都是空气的污染物)3Cu+8HNO3(稀)=3... -
禹关味13359959257 ______[答案] (1)用铜屑和浓硝酸、稀硝酸为原料制取硝酸铜分别生成了二氧化氮、一氧化氮,都属于空气的污染气体,污染了环境;由反应的化学方程式可知:Cu~4HNO3(浓),3Cu~8HNO3(稀),制备等质量的硝酸铜时消耗的稀硝酸比...