铁碘原电池图示
【来源:哈尔滨工业大学新闻网_学校要闻】
哈工大全媒体(张子帅 文/图)近日,我校化工与化学学院于淼教授团队与深圳校区黄燕教授团队在水系碘电池研究方面取得重要进展,研究成果以《长寿命高性能水系有机||碘二次电池的突破》(Development of long lifespan high-energy aqueous organic||iodine rechargeable batteries)为题发表在《自然通讯》(Nature Communications)上。团队首次提出水系碘正极串联电池概念,通过采用有机电极材料作为电池负极,在饱和氯化钾/碘混合溶液中构建了水系碘正极串联电池,为水系电池碘正极材料充放电过程中的穿梭效应问题提供有效解决方法。
近年来,基于氧化还原化学反应机制来获得具有高能量密度和高功率密度的可充电金属||卤素电池引起人们广泛关注。由于其具有储量丰富、理论容量高、理论氧化还原电位高的优势,碘成为有发展潜力的水系电池正极材料。此外,碘正极的I−/I0/I+固/液转化反应也避免其在其他嵌入/脱出机制材料中出现常见的电极结构退化问题。然而,金属负极的枝晶生长和腐蚀会导致出现电池容量的快速衰减和短路;碘阴离子与金属负极形成的非电化学活性产物也会导致出现碘正极不可逆程度增加和循环寿命缩短,产生类似锂/硫电池体系中的穿梭效应。
团队首次提出水系有机负极||碘串联电池的概念(如图),采用苝四甲酰二亚胺(PTCDI)作为负极活性材料、饱和氯化钾和碘混合溶液作为电解液。这些成分的使用可在一个电化学储能装置中实现接续发生两个可逆电化学反应。当以活性炭包覆的碘单质为正极材料组装成全电池后,电池体系可在40安/克的电流密度下获得900毫安时/克(以电极材料中的碘为基础)的初始放电容量和1.25伏的平均放电电压。此外,该文还报道了水系无正极碘基软包电池的组装和测试,该电池在80毫安的电流下经历900次循环后,放电容量仍能保持约70%。该研究解决了水系碘正极电池面临的主要问题,丰富了水系卤素电池的研究范围,并为基于硫电极的高性能电池体系的构建提供新研究思路。
我校化工与化学学院博士生张子帅为论文第一作者。阿德莱德大学化工与先进材料学院博士研究生朱奕龙为论文第二作者。于淼教授、阿德莱德大学焦研教授、黄燕教授为共同通讯作者。
论文链接:
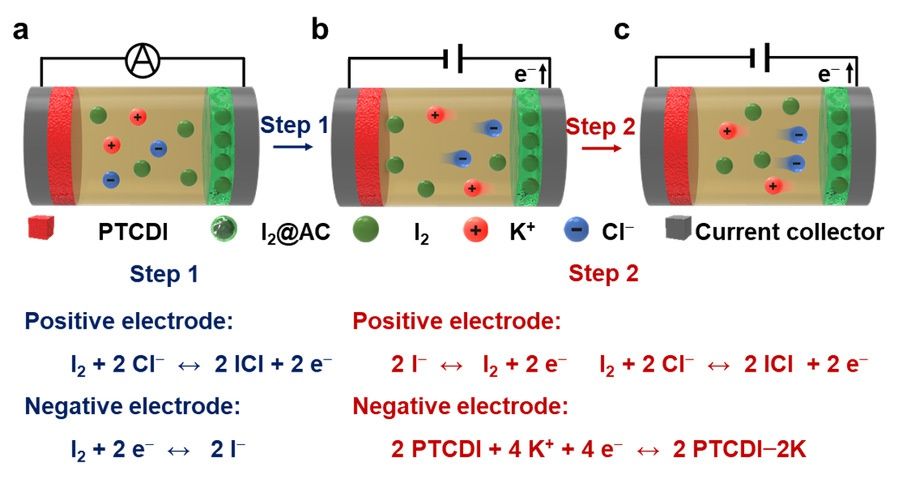
水系PTCDI||I2串联电池的未循环状态(a)、第一步充电状态(b)和第二步充电状态(c)示意图
声明:此文版权归原作者所有,若有来源错误或者侵犯您的合法权益,您可通过邮箱与我们取得联系,我们将及时进行处理。邮箱地址:[email protected]
","force_purephv":"0","gnid":"989ca515ba7d2159f","img_data":[{"flag":2,"img":[{"desc":"","height":"481","title":"","url":"https://p0.ssl.img.360kuai.com/t01ed83376cff8037a4.jpg","width":"898"}]}],"original":0,"pat":"art_src_1,fts0,sts0","powerby":"hbase","pub_time":1668838774000,"pure":"","rawurl":"http://zm.news.so.com/ab4e64fa301534682f6d1e2061f3983f","redirect":0,"rptid":"8e1ddc46c9e46a69","s":"t","src":"九派教育","tag":[{"clk":"kscience_1:自然通讯","k":"自然通讯","u":""}],"title":"化工与化学学院于淼教授团队在水系碘电池研究方面取得重要进展
娄珠菁3345铁 硫酸铁 碳 如何形成原电池 -
戈毅陈17656798601 ______ 负极材料:铁 Fe-2e-=Fe2+ 正极材料:石墨 2Fe3++2e-=2Fe2+ 电解液:硫酸铁溶液 总反应:2Fe3++Fe=3Fe2+
娄珠菁3345如图为原电池装置示意图:(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A电极名称为 - -----,写出正极 -
戈毅陈17656798601 ______ (1)该原电池中,锌失电子变成离子进入溶液,所以锌极即A极为负极,石墨为正极,正极上氢离子得电子生成氢气,所以电极反应式为2H++2e-=H2↑. 故答案为:负极;2H++2e-=H2↑;(2)该原电池中,铁片失电子变成二价铁离子进入溶液,电极反...
娄珠菁3345铁,碘原电池该怎麽设计啊? -
戈毅陈17656798601 ______ 题主:应该是铁碳原电池,碘貌似不合适做电极吧? 铁碳原电池:以铁棒和碳棒做电极,用导线将两电极连接,插入盛装有饱和氯化钠溶液的容器中就OK了
娄珠菁3345铁和锌原电池,电解液为氯化钠,电极反应方程式如何写 -
戈毅陈17656798601 ______ 锌在空气中不易被氧化,而铁在氯化钠溶液(电解质)存在的情况下较容易发生氧化反应(铁生锈反应).所以,具体的电极方程式应该是:负极(铁电极):2Fe - 4e⁻ = 2Fe²⁺ 正极(锌电极):O₂+ 4e⁻ + 2H₂O = 4OH⁻ 总反应式:2...
娄珠菁3345某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu.(1)将上述反应设计成的原电池如图甲所示,请回答 -
戈毅陈17656798601 ______ (1)①据反应物和生成物可以确定该反应为2FeCl3+Cu═2FeCl2+CuCl2,所以X为FeCl3和FeCl2溶液,故答案为:FeCl3和FeCl2; ②Cu做负极,发生的电极反应为Cu-2e-═Cu2+,故答案为:Cu-2e-═Cu2+; (2)①根据转移电子的物质的量和金属阳离...
娄珠菁3345下列关于如图所示的原电池装置的说法正确的是 -
戈毅陈17656798601 ______ 看不到图,如果没猜错的话此题应该是铁、铜做电极、以硫酸铜做为电解液的原电池.1、铁释放电子变为铁离子,为负极;铜离子接收电子还原成铜,为正极2、溶液中的铜离子(蓝色)逐渐减少,铁离子(黄色)逐渐增多 所以选项A正确
娄珠菁3345铁和碳与NACL构成原电池的正负极反应原理 -
戈毅陈17656798601 ______ 以铁为负极,碳棒为正极,NaCl溶液为电解质溶液,则空气中的氧气溶解在电解质溶液中,并在正极放电,则铁在负极放电从而电极反应式为 负极 Fe-2e-=Fe2+ 正极O2+4e-+2H20=4OH- 因而在电极中间还会形成少量白色Fe(OH)2沉淀
娄珠菁3345锌和铁做电极,氯化钠为电解质溶液,构成的原电池的原理及方程式, -
戈毅陈17656798601 ______ 吸氧腐蚀 (-)2Zn - 4e- == 2Zn2+ (+)O2 + 2H2O + 4e- == 4OH- Zn2+ + 2OH- == Zn(OH)2
娄珠菁3345铁,铜,稀盐酸能否构成原电池
戈毅陈17656798601 ______ 可以,构成原电池就由三个部分构成,⑴两种活泼性不同的金属 ⑵电解质 ⑶成为一个闭合的通路 只要将铁和铜同时放进稀盐酸里,外面用导线连着就行(或者两个金属相互接触) 就能构成原电池了
娄珠菁3345锌铜原电池装置如图所示,常常采用电池图式表达式,如:Zn|ZnSO4(1mol/L)‖CuSO4(1mol/L)|Cu上式中,负极写在左边,发生 - __反应,正极写在右边.用... -
戈毅陈17656798601 ______[答案] 该原电池中,锌易失电子发生氧化反应作负极,铜作正极;在电池甲,正极上三价铁离子得电子生成二价铁离子2Fe3++2e-═2Fe2+, 故答案为:氧化反应;2Fe3++2e-═2Fe2+.