铵根离子成键方式
以电池为能量来源的手机、电脑、平板等已经成了我们生活的一部分,越来越多的人开始患上“电量焦虑症”,同时,新能源汽车的加速普及也让人们对充电耗时长的电池越来越难以忍受——快点!电池充得再快一点!这成了所有人共同的心愿。

电量焦虑成了这个时代焦虑来源之一。图库版权图片,转载使用可能引发版权纠纷
这个心愿可能很快就要实现了。最近,中国科学技术大学国家同步辐射实验室教授宋礼团队开发出了一种具有快充能力的电池。
今天我们就来仔细地聊一聊这项科研成果。
锌离子电池 VS 锂离子电池
锂离子电池是目前大家所广泛认识的一种储能器件。凭借能量密度高、工作温度范围广等优势,锂离子电池已占据商业化电池中绝大部分份额。但是,其中所使用的有机电解液对人体有一定危害,而且锂资源短缺的问题会导致电池市场在未来出现供不应求的状况。
而锌离子电池作为储能界的新秀,既具有较高的理论能量密度,还具有无毒性的水系电解液,保证了安全、高效的生产与应用。另外,廉价且丰富的锌资源也大大降低了电池的使用成本,有望在未来成为锂离子电池的潜在替代品。
即便在材料的使用上有诸多不同,但锌离子电池和锂离子电池在充放电过程的工作状态却是很类似的。
电池的正极材料往往是层状的:在电池的放电过程中,锂离子(或锌离子)将嵌入正极材料的层间进行储存;而在电池的充电过程中,锂离子(或锌离子)会从正极材料层间脱出,回到负极。
总体来看,电池的工作原理就是一个由离子迁移与电子转移共同作用的过程。

锂离子电池。图库版权图片,转载使用可能引发版权纠纷
电池快充的原理
那么在这项科研成果中,快速充电的电池是如何实现的呢?
拓宽离子传输通道
正如上文所说的,锌离子电池的充放电过程就是一个离子不断迁移的过程。如果想要在短时间内储存尽可能多的电池容量,就得给锌离子创造一个较大的储存空间。
首先,研究者将目光聚焦在空间结构可调的层状五氧化二钒材料上。这种层状五氧化二钒材料的结构就像由多个平行的板子排列而成的。为了增加层状正极材料的层间距,可以预插层尺寸较大的铵根离子。这也就是预先在这些层之间加上一些支柱,来增加层间距。
有了铵根离子的支撑,锌离子就可以更容易地在正极材料中进行迁移,而且更大的层间空间,也可以有效提高电池的储能容量。
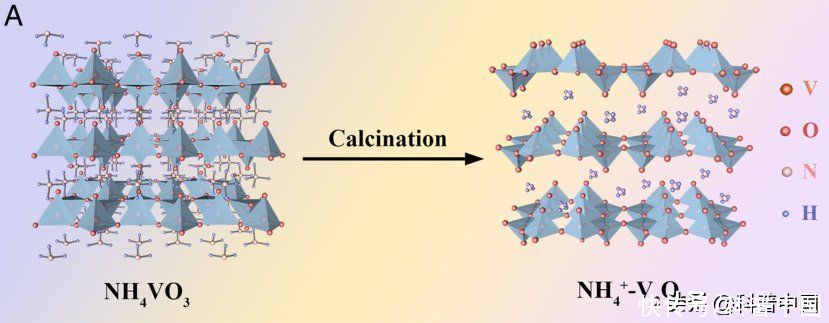
铵根插层五氧化二钒结构示意图。图片来源:参考文献 [1]
从调整轨道占据到加速电子转移
要知道电池的储能过程与离子迁移、电子转移密切相关。当锌离子进入正极材料层间进行储存时,一部分电子也将转移至正极材料来保持整体的电荷平衡。所以研究插层离子对层状材料电子结构的影响也十分重要。
但传统的测试手段很难清晰地探索材料内在的原子和电子结构。因此,需要使用更加先进的同步辐射表征技术来进行探测。简单来说,我们可以将同步辐射技术理解成一个加强版的“超级显微镜”,利用其高亮度和宽波段的特点可以看清物质内部的结构。
通过这种技术,研究者们探究了在层间插入铵根离子支柱后,五氧化二钒材料中原子轨道占据的变化以及在充放电过程中的可逆演变规律。
在这里我们先介绍一下基本的电子结构概念。
对于含有核外电子的元素,它们所带的电子都不是杂乱排布的,而是依次排布在轨道上。并且,电子总是先占据能量低的轨道,也就是以原子核为中心,由内而外地进行排布。
对于钒元素而言,它的价电子排布式如下图,外层含有 5 个价电子。在五氧化二钒材料中,这 5 个电子都用于和氧原子成键。此时,钒的 3d 轨道就是未被电子占据的空轨道。

钒元素。图库版权图片,转载使用可能引发版权纠纷
在同步辐射技术的帮助下,研究者清晰地看到,铵根离子支柱的插入,使五氧化二钒的晶体结构发生畸变,并改变了原本的 V-O 键键长。最重要的是,这种结构的畸变也改变了钒的电子结构,使电子跃迁到原本空的 V3d 轨道,导致 V3d 轨道处于部分占据的状态。然而这一部分的电子并没有服务于氧原子,而是显著提高了材料的导电性。
结合前文所说,在电池充放电过程中,既存在离子迁移,也存在电子转移。通过同步辐射表征显示,经过铵根离子插层的五氧化二钒正极材料在充放电过程中体现出可逆演变规律。在放电时,电子转移至正极材料,带来了 V3d 轨道的进一步占据,而充电时,电子脱离,V3d 轨道又能恢复到原本的占据状态。然而这种轨道占据的可逆变化并未在原本的五氧化二钒材料中观察到。
总结来看,电子结构的变化不仅使导电性提高,大大加速电荷的流动,还能使电池充放电的可逆性提升,进一步结合层间距拓宽对锌离子迁移的加速作用,共同实现了电池的快速充电特性。
晶体结构与电子结构的双重调控,使快速充电、稳定循环走入现实
当使用这种新型正极材料时,锌离子电池在 200C 的电流密度下,实现了 101mAh/g 的容量,并且充电仅需 18s。同时,其中的水系电解液也保证了循环过程中的安全性,减少了对环境的污染。
论文从材料晶体结构和电子结构两方面出发,设计并调控了层状材料的层间距和轨道占据状态。同时,结合了先进的同步辐射表征手段,更加直观、清晰地说明了材料结构上的演变,使具有快速充电特性的正极材料成为可能。
也许在不久的未来,这类材料能够应用到电子产品,乃至公共交通。充电时间的大幅降低,能够让人们的生活更加高效、便捷;电池材料的安全、清洁,也能减少给环境的负担。相信科技会让这一天不再遥远。
参考资料
[1] Yixiu Wang, Shiqiang Wei, Zheng-Hang Qi, et al. Intercalant-induced V t2g orbital occupation in vanadium oxide cathode towards fast-charging aqueous zinc-ion batteries. PNAS, 2023, 120, e2217208120.
策划制作
出品|科普中国
作者|董少祥 王一琇 中国科学技术大学
监制|中国科普博览
","gnid":"9517211efcf39041a","img_data":[{"flag":2,"img":[{"desc":"","height":"721","title":"","url":"https://p0.ssl.img.360kuai.com/t01048cd4dbff33c7d3.jpg","width":"1080"},{"desc":"","height":"723","title":"","url":"https://p0.ssl.img.360kuai.com/t0105a0e6e0db385b3a.jpg","width":"1080"},{"desc":"","height":"323","title":"","url":"https://p0.ssl.img.360kuai.com/t01b57588ace83be35b.jpg","width":"829"},{"desc":"","height":"1000","title":"","url":"https://p0.ssl.img.360kuai.com/t01ad79f922b163db20.jpg","width":"1000"}]}],"original":0,"pat":"qgc,art_src_3,fts0,sts0","powerby":"hbase","pub_time":1691999160000,"pure":"","rawurl":"http://zm.news.so.com/11be605a7bb8eeda881835877f6c610b","redirect":0,"rptid":"0b9893b6d7d62ffe","rss_ext":[],"s":"t","src":"科普中国","tag":[{"clk":"kdigital_1:锂离子电池","k":"锂离子电池","u":""},{"clk":"kdigital_1:电子","k":"电子","u":""}],"title":"18 秒就能充满电?!再也不用担心出门手机没电了……
易狄选5191铵根离子中N一H键长与氨气中N一H键长 -
彭削时18646528903 ______ (1)铵根的四个键中有三个是普通共价键,有一个是配位键.但铵离子一旦生成,这四个键就不存在任何差别了.其键长、键能均相等.(2)配位键:指的是形成这条成化学键时原子是由其中的一个原子单独提供的共价键.正常的单键是形成这条成化...
易狄选5191含铵根离子和金属离子的是什么键?是离子键还是共价键?共价键的离子化合物又是什么? -
彭削时18646528903 ______[答案] 含铵根离子的是离子键,含金属离子的也是离子键(金属单质是金属键) 含共价键的离子化合物如含氧酸盐、强碱、铵盐等
易狄选5191铵根离子在形成时是哪个原子失去了一个原子啊? -
彭削时18646528903 ______ 铵根离子在形成机理是NH3分子和H+结合,生成铵根离子.
易狄选5191铵根离子中存在的化学键类型按离子键、共价键和配位键分类,应含有 ( ) A.离子键和共价键 B. -
彭削时18646528903 ______ 答案:C 铵根离子中N原子最外层5个电子,采用sp3杂化形成4个杂化轨道,其中一个杂化轨道被孤对电子占据,与H+的空轨道形成配位键;另三个轨道与H形成共价键
易狄选5191氨根离子中都是共价键吗 -
彭削时18646528903 ______ 从氨分子的电子式可以看出,氨分子的氮原子周围还有一对未共用电子,而氢离子的周围正好是空的.当氨分子和氢离子相遇时,它们一拍即合,即氢离子和氨分子结合时各原子周围都是稳定结构.这样,在氮原子和氢离子之间又新成了一种新...
易狄选5191离子键的成键粒子和成键方式,和成键元素. -
彭削时18646528903 ______ 成键粒子是离子,成键方式高中没学.元素应该是金属元素为阳离子,非金属阴离子,或者离子团做阴离子,特殊的有铵根离子非金属做阳离子
易狄选5191氨根离子中都是共价键吗氨气中3个H分别与N共用一对电子,N达到8电子稳定结构,那NH4中第4个H与N是形成共价键吗? -
彭削时18646528903 ______[答案] 从氨分子的电子式可以看出,氨分子的氮原子周围还有一对未共用电子,而氢离子的周围正好是空的.当氨分子和氢离子相遇时,它们一拍即合,即氢离子和氨分子结合时各原子周围都是稳定结构.这样,在氮原子和氢离子之间又新成了一种新的共价...
易狄选5191铵根离子中心原子轨道杂化方式如题,还有是怎么知道的? -
彭削时18646528903 ______[答案] 氨分子是采用SP3等性杂化轨道,形成近乎正四面体的结构.氮原子上已成对的两个电子占据了一个杂化轨道,另三个杂化轨道与三个氢形成共价键结合,那么铵离子(正一价)就是正一价氢与氨中氮原子上的孤对电子配位
易狄选5191离子键的形成条件 -
彭削时18646528903 ______ 1. 元素的电负性差比较大 X > 1.7,发生电子转移,产生正、负离子,形成离子键; X 1.7 ,实际上是指离子键的成分大于 50 %) 2. 易形成稳定离子 Na + 2s 2 2p 6,Cl- 3s 2 3p 6 , 只转移少数的电子就达到稀有气体式稳定结构. 3. 形成离子键时释放能量多 Na ( s ) + 1/2 Cl 2 ( g ) = NaCl ( s ) H = -410.9 kJ·mol-1 在形成离子键时,以放热的形式,释放较多的能量.
易狄选5191化学中的氨、胺、铵,怎么区别呀?
彭削时18646528903 ______ 1、氨是氮和氢的一种化合物,分子式为NH 3 . 2、 铵是从氨衍生所得的带一个单位正电荷的离子,化学式为NH 4 + ,四个N-H键的键长、键能、键角完全相同,离子的空间构型为正四面体型. 3、胺是氨的氢原子被烃基代替后的有机化合物.氨分子中的一个、两个或三个氢原子被烃基取代而生成的化合物. 其性质也不同: 1、氨是一种无色、有臭味的气体,易溶于水.氨能够单独存在. 2、铵相当于正一价金属阳离子,凡是含NH4+的盐叫铵盐.NH4+不能单独存在,只能在铵盐或氨水中与阴离子共存. 3、胺类广泛存在于生物界,具有极重要的生理作用.